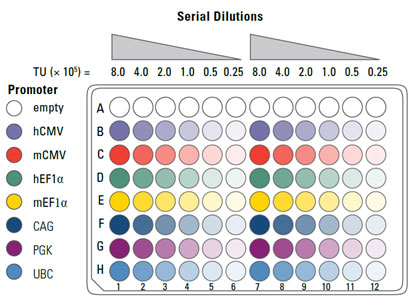
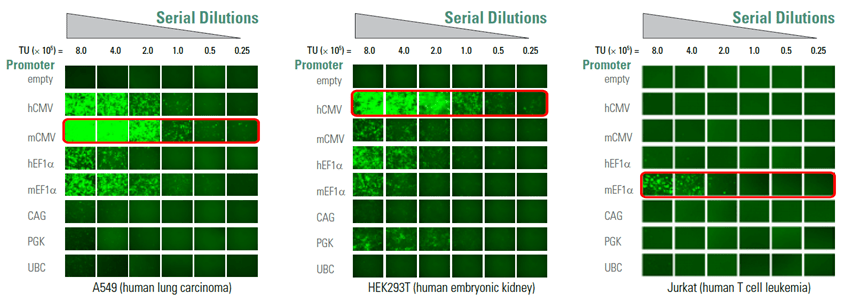
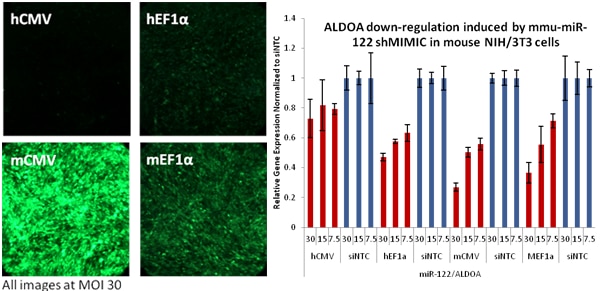
SMARTchoice promoter selection plate
目的の細胞における発現を積極的に駆動するプロモーターを簡単に定性的に評価できる画期的なツール
SMARTchoice Promoter Selection Plateを使用して目的の細胞に最適なプロモーターを特定することで、レンチウイルスshRNAおよびshMIMIC microRNAの機能と性能を向上させることができます。その結果、形質転換された初代胚性幹細胞や神経細胞など、目的の細胞で遺伝子のダウンレギュレーションが成功します。