- CRISPRa (CRISPR activation) 試薬
- CRISPRa all-in-one lentiviral sgRNA
CRISPRmod CRISPRa all-in-one lentiviral sgRNA
簡便なデリバリーおよび効率的な遺伝子活性化または過剰発現のためのマウスおよびヒト用dCas9-VPRとsgRNAの単一発現ベクター
- より簡単なデリバリーですぐに使えるレンチウイルス粒子(解凍後レンチウイルスを細胞に加えるだけ)
- 単一試薬の導入で結果までの時間を短縮可能
- トランスフェクションが困難な細胞や継代数の少ない細胞に最適
- ピューロマイシン耐性またはEGFP蛍光による濃縮が可能
- transduction-ready試薬は、クローニングやin vitro転写のステップを必要としません。


1Start Here
2Choose
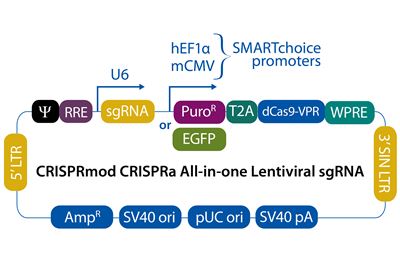
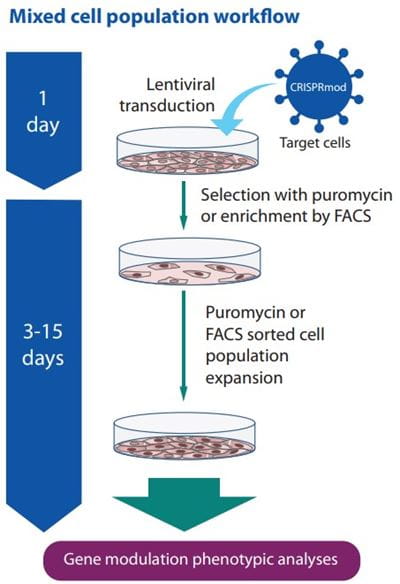
CRISPRmod CRISPR activation (CRISPRa)システムで目的の遺伝子の転写を活性化し、安定細胞株を容易に作製することができます。このシステムは古典的なCRISPR-Cas9遺伝子編集システムのユニークな応用であり、触媒機能が不活性化されたCas9(deactivated Cas9: dCas9)を3成分からなる活性化因子(VPR)と融合して利用します。プロモーター領域や転写開始部位(transcriptional start site: TSS)付近の配列を標的として設計されたガイドRNAと組み合わせると、遺伝子転写を活性化することができます。
ピューロマイシン耐性遺伝子またはEGFPマーカーを選択することで、ベクターの統合に成功した細胞を選択することができます。EGFP選択マーカーは、蛍光が発現するとすぐにFACS分析が行えるので、編集細胞をすぐに濃縮したい場合にご利用いただけます。これは、初代細胞のような寿命の短い細胞タイプに特に適しています。
デザイン済みのall-in-one CRISPRa lentiviral sgRNAの特長:
- 最低限の細胞毒性で直接導入するための高品質、濃縮、精製されたレンチウイルス粒子(力価:1 x 107 TU/mL以上)
- Horlbeckらにより報告されたアルゴリズムにより最適化されたデザインは、強力な遺伝子活性化を示します(Referencesタブを参照)。
- 異なる転写開始部位を持つ遺伝子には、別のガイドRNAデザインも利用可能(P2と表示)
技術概要は、CCRISPRaアプリケーションのページ、またはall-in-one CRISPRアプリケーションのページをご覧ください。
CRISPRa all-in-one lentiviral sgRNAコントロール
CRISPRa all-in-one lentiviral sgRNAポジティブコントロール
- 十分に特徴付けられた遺伝子を標的とするall-in-one Lentiviral sgRNAであり、遺伝子転写活性化の効率を最大化するための実験条件の検討、および最適化の確認のために使用します。
CRISPRa all-in-one lentiviral sgRNA non-targetingコントロール
- バイオインフォマティクスに基づき設計されたall-in-one non-targeting sgRNAコントロールは、標的遺伝子特異的sgRNAの非存在下でCRISPRaコンポーネントに対するベースラインの細胞応答を評価するために使用します。
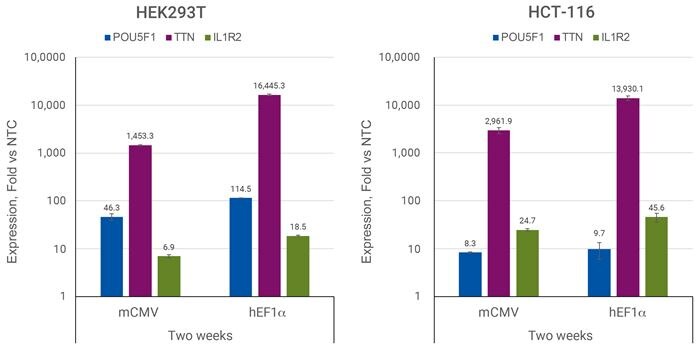
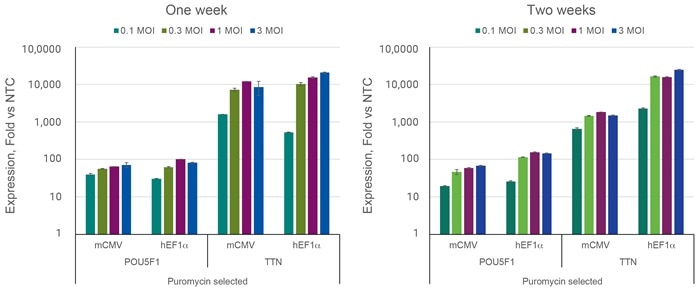
- M. A. Horlbeck et al., Compact and highly active next-generation libraries for CRISPR-mediated gene repression and activation. eLife. 5, e19760 (2016).
LentiBOOST Lentivirus Transduction Enhancer is a uniquely formulated transduction reagent that can be used with or without lentivirus spinfection in order to increase successful viral transduction events while preserving cell viability. Especially critical for preserving precious primary cells from patient cohorts, or, for engineering complex animal models; improving transduction efficiency can save time and costs by increasing the success of each editing/transduction step, or, even avoid the loss of irreplaceable samples. Additionally, LentiBOOST technology is already used in the manufacturing of a number of clinical stage therapies providing the opportunity to demonstrate improved workflow applicability to the clinic.
LentiBOOST can be purchased through the Dharmacon Reagents catalog.
To learn more about LentiBOOST technology visit the Revvity LentiBOOST webpage.
Supporting Data
Improved CD8+ T-cell SMARTvector™ shRNA lentiviral system transduction using LentiBOOST™ Lentivirus Transduction Enhancer
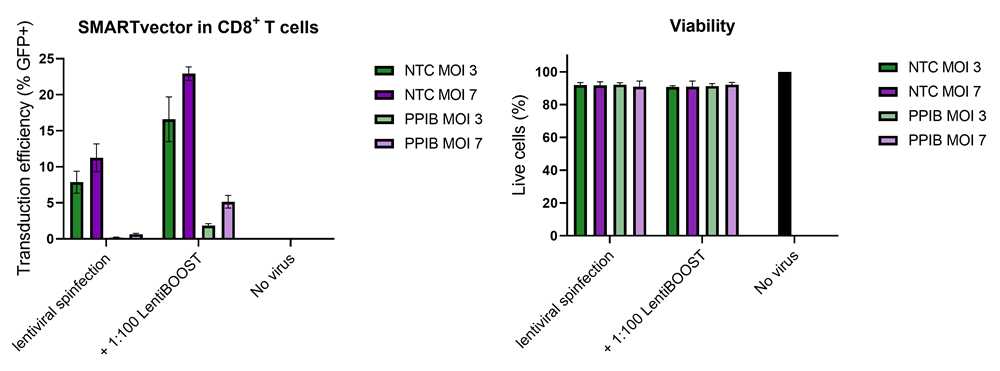
100,000 primary human CD8+ T cells were transduced with either 30,000 (MOI 3, green) or 70,000 (MOI 7, purple) TUs of SMARTVector™ mCMV tGFP Lentiviral Control Particles targeting either NTC or PPIB along with 1:100 LentiBOOST transduction enhancer. Cells were centrifuged at 800 x g for one hour at 32 °C followed by a four hour incubation prior to removal of lentiviral particles and transduction enhancer. Transduction efficiency (%GFP+ out of live cells) and viability were determined 5 days post-transduction by flow cytometry. The addition of LentiBOOST technology markedly improved transduction efficiencies without significantly impacting cell viability.
Improved CD4+ and CD8+ T-cell Edit-R™ All-in-one sgRNA/Cas9 lentiviral system transduction using LentiBOOST™ Lentivirus Transduction Enhancer
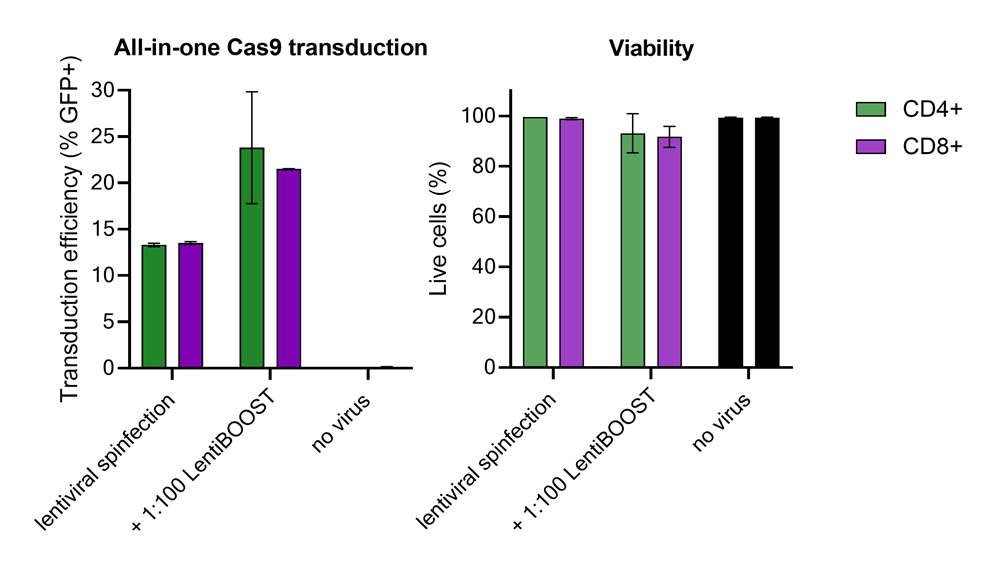
100,000 primary human CD4+ and CD8+ T cells from two donors were transduced with 250,000 TUs of Edit-R GFP Delivery controls mCMV along with 1:100 LentiBOOST transduction enhancer. Cells were centrifuged at 800 x g for one hour at 32 °C followed by an overnight incubation prior to removal of lentiviral particles and transduction enhancer. Transduction efficiency and viability were determined 72 hours post-transduction by flow cytometry. The addition of LentiBOOST technology markedly improved transduction efficiencies without significantly impacting cell viability.
Improved transduction of human induced pluripotent stem cells (hiPSCs) with the Strict-R™ Inducible CRISPRa lentiviral system transduction using LentiBOOST™ Lentivirus Transduction Enhancer

10,000 WTC hiPS cells were transduced with either 20,000 (MOI 2, green) or 40,000 (MOI 4, purple) TUs of Strict-R™ Inducible EGFP dCas9-VPR Lentiviral Particles along with 1:100 LentiBOOST transduction enhancer. Cells were centrifuged at 800 x g for one hour at 32 °C followed by an overnight incubation prior to removal of lentiviral particles and transduction enhancer. Transduction efficiency and viability were determined 72 hours post-transduction by flow cytometry. The addition of LentiBOOST markedly improved transduction efficiencies without significantly impacting cell viability.
Product inserts
Protocols
Safety data sheets
Selection guides
Related Products
バイオインフォマティックに基づいて設計され、ヒトまたはマウスゲノム中のどの遺伝子も標的としないことが検証されているall-in-oneのnon-targetingコンストラクト
CRISPRa all-in-one lentiviral sgRNAポジティブコントロールは、目的の細胞タイプにおけるCRISPR遺伝子転写活性化の効率を最大化するための実験条件の検討、および最適化の確認のために使用します。
LentiBOOST transduction enhancer can increase successful viral transduction in challenging to transduce cells, or, complex cellular engineering work; while preserving cell viability and minimizing the amount of viral particles required for your experiment. LentiBOOST technology is actively used in the production of clinical stage lentivirally delivered therapies, including some approved therapies, providing a direct path to therapeutic applicability for your research studies. Tested with Dharmacon Lentiviral reagents.
信頼性の高い遺伝子活性化に必要なすべてのコンポーネントを単一試薬に組み合わせることにより、コストのかかるインフラを必要とせずに、偏りのない表現型機能獲得スクリーニングを実施できます。
