- CRISPRa (CRISPR activation) 試薬
- Strict R Inducible CRISPRaレンチウイルスシステム
Strict R Inducible CRISPRaレンチウイルスシステム
精密な遺伝子活性化を可能にする二重誘導制御:仕組み
System OFF:ドキシサイクリンおよびShield1が存在しない場合、本システムは不活性状態を維持します。TRE3Gプロモーターからの残存的な転写によりデグロンタグ付きdCas9 VPRが産生された場合でも、当該タンパク質は速やかにプロテアソーム分解を受けるため、意図しないバックグラウンド活性化は最小限に抑えられます。
System ON:ドキシサイクリンの添加によりTet On 3Gトランスアクチベーターが活性化され、dCas9 VPRの強力な発現が誘導されます。さらにShield1を添加することで、発現したdCas9 VPRタンパク質が安定化され、蓄積が可能となり、精密な遺伝子活性化が実現されます。
Dharmacon Strict R Inducible CRISPRaレンチウイルスベクターの模式図
Dharmacon Strict R 誘導型 CRISPRaレンチウイルスシステムによる転写レベルおよび翻訳後レベルでの制御

Strict R Inducible Lentiviral CRISPRaシステムの模式図を示しています。ドキシサイクリンおよびShield1非存在下では、本システムは「OFF」状態となります。TRE3Gプロモーターからのリーキーな転写により、FKBP12由来の不安定化ドメイン(デグロン)と融合したdCas9 VPRが翻訳されますが、当該タンパク質は速やかにプロテアソーム分解を受けます。ドキシサイクリンの添加によりTRE3Gプロモーターからの強力な転写が誘導され、さらにShield1の添加によってdCas9 VPRが安定化されることで、遺伝子特異的sgRNA存在下において高効率な標的遺伝子活性化が可能になります。本図はBioRender.comを用いて作成されています。
Highlights
- 低分子誘導による可逆的な標的遺伝子活性化
- dCas9‑VPR融合タンパク質による高効率な転写活性化と低いオフターゲット影響
- ドキシサイクリンおよびShield1添加により迅速なdCas9‑VPR発現誘導を可能にするTet‑デグロンシステム
- 単一のレンチウイルスベクターによる発現で、既存の実験ワークフローに容易に統合可能
- 遺伝子発現解析、機能ゲノミクス、スクリーニング、治療応用研究など幅広い用途に対応
- 高品質・精製済みレンチウイルス粒子を低細胞毒性で直接導入可能(力価:≥1 × 10⁷ TU/mL)
- ブラスチジン選択またはEGFP蛍光レポーターの選択肢を用意
Strict R Inducible Lentiviral CRISPRaシステムを用いた遺伝子活性化ワークフロー

図1:Strict R Inducible Lentiviral CRISPRaシステムを用いた遺伝子活性化ワークフロー
Strict-R Inducible Lentiviral CRISPRaシステムによる遺伝子活性化のより厳密な制御
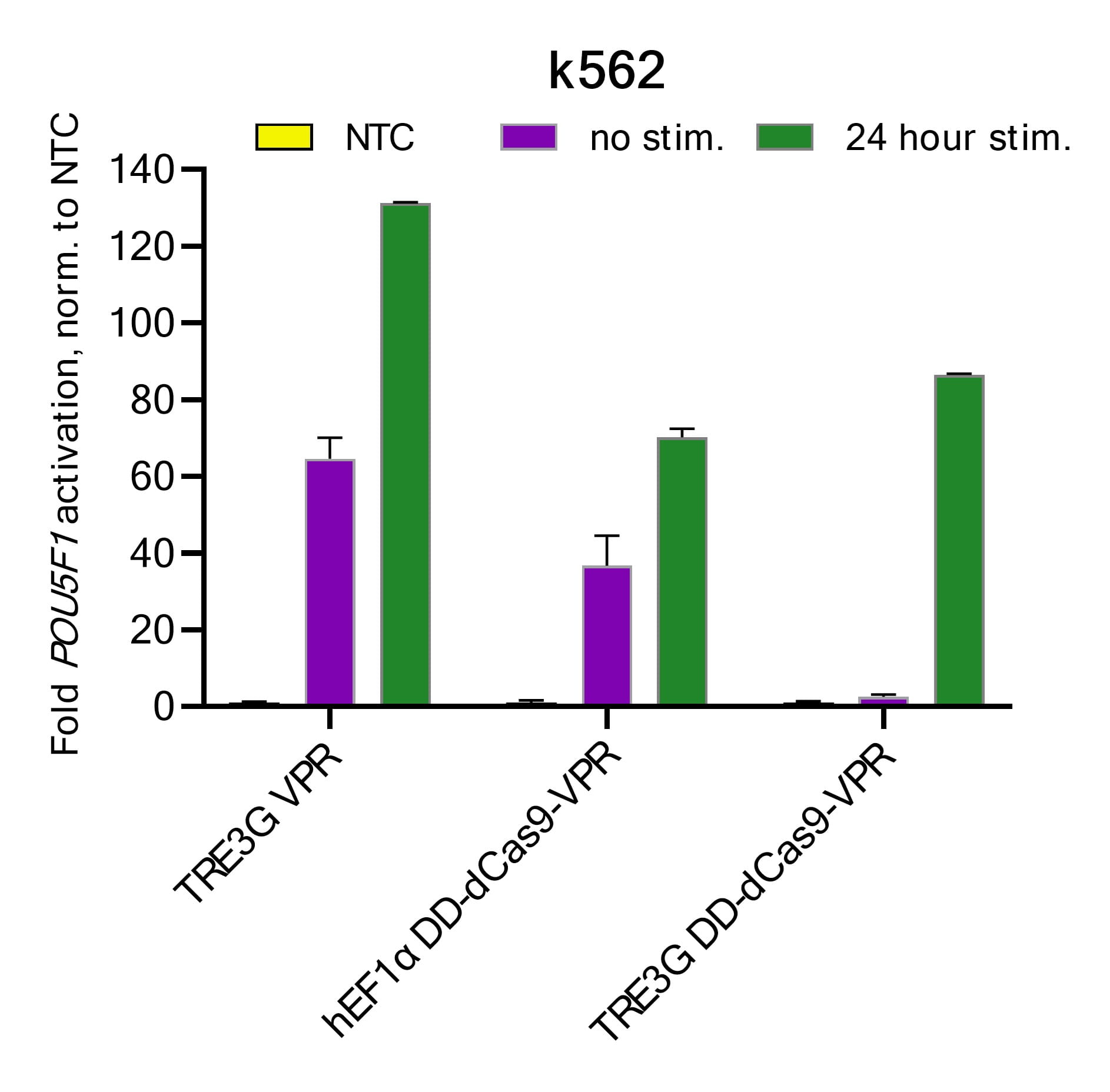
図1:K562細胞に、各dCas9 VPR構築体を含むレンチウイルス粒子をMOI <0.3で導入しました。細胞は10 µg/mLブラスチジンで2週間選択し、3〜4日ごとに継代しました。ブラスチジン選択後、安定細胞株に対して、POU5F1を標的とするCRISPRmod CRISPRaレンチウイルスsgRNA、または非標的コントロール(NTC)をMOI 0.3で導入しました。48時間後、2.5 µg/ mLピューロマイシンで5日間選択を行いました。細胞を96ウェルプレートに1ウェルあたり20,000細胞で播種し、回収24時間前に0.5 µg/mLドキシサイクリンおよび0.25 nM Shield1で刺激しました。全RNAを抽出し、RT qPCRにより相対遺伝子発現量を測定しました。POU5F1の相対発現量は、ACTBをハウスキーピング遺伝子としてΔΔCq法により算出し、NTCに対してノーマライゼーションしました。Strict R Inducible Lentiviral CRISPRaシステムでは、未刺激条件におけるバックグラウンド遺伝子活性化(リーク性、紫)が大幅に低減される一方、2種類の細胞透過性に優れた低分子化合物添加により、強力な標的遺伝子活性化が可能となりました。
Strict-R Inducible Lentiviral CRISPRaシステムは、複数の細胞株および遺伝子標的において、強力な活性化と最小限のリーク性を示す

図2:U2OS、HeLa、ヒト人工多能性幹細胞(hiPSC)に、Strict R Inducible Lentiviral CRISPRaシステム、または構成的hEF1αプロモーター制御下のdCas9 VPR(黒)を発現させました。これらの細胞に、EGFRまたはASCL1を標的とするCRISPRmod™ CRISPRaレンチウイルスsgRNA、または非標的コントロール(NTC)をMOI 0.3で導入しました。48時間後、2.5 µg/mLピューロマイシンで5〜7日間選択を行いました。細胞を96ウェルプレートに1ウェルあたり20,000細胞で播種し、回収48時間前に0.5 µg/mLドキシサイクリンおよび0.25 nM Shield1で刺激しました。全RNAを抽出し、RT qPCRにより相対遺伝子発現量を測定しました。各遺伝子の相対発現量は、ACTBをハウスキーピング遺伝子としてΔΔCq法により算出し、NTCに対してノーマライゼーションしました。Strict R Inducible Lentiviral CRISPRaシステムでは、刺激48時間後に強力な標的遺伝子発現上昇が認められ、構成的dCas9 VPRシステムと同等のレベルに達しました。一方、未刺激条件ではバックグラウンド活性化は最小限に抑えられていました。
FACSによるEGFP高発現Strict-R InducibleレンチウイルスCRISPRa陽性Jurkat細胞の選別と高いCRISPRa活性集団の取得

図3:Jurkat細胞にStrict R Inducible Lentiviral CRISPRa EGFP粒子をMOI <0.3で導入しました。細胞を増殖させた後、FACSにより蛍光強度に基づいてGFP lowおよびGFP hiの2集団に分取しました。分取後、細胞を6ウェルディッシュに再播種し、回復および増殖させました。その後、EGFRまたはPOU5F1を標的とするCRISPRmod CRISPRaレンチウイルスsgRNA、または非標的コントロール(NTC)をMOI 0.3で導入しました。48時間後、2.5 µg/mLピューロマイシンで5日間選択を行いました。細胞を96ウェルプレートに1ウェルあたり20,000細胞で播種し、回収48時間前に0.5 µg/mLドキシサイクリンおよび0.25 nM Shield1で刺激しました。全RNAを抽出し、RT qPCRにより相対遺伝子発現量を測定しました。各遺伝子の相対発現量は、ACTBをハウスキーピング遺伝子としてΔΔCq法により算出し、NTCに対してノーマライゼーションしました。刺激48時間後、GFP hi集団ではより高い標的遺伝子活性化が認められました。一方、未刺激条件におけるGFP lowおよびGFP hi集団のいずれにおいても、バックグラウンド活性化は最小限であり、高発現細胞の濃縮が背景活性の増加につながらないことが示されました。
薬剤誘導によるASCL1の活性化は、hiPSCsにおいて下流標的であるDLL1およびDLL3の発現上昇を引き起こす

図4:Strict R Inducible Lentiviral CRISPRaシステムを発現するhiPSCに、ASCL1を標的とするCRISPRmod CRISPRaレンチウイルスsgRNA、または非標的コントロール(NTC)をMOI 0.3で導入しました。48時間後、2.5 µg/mLピューロマイシンで7日間選択を行いました。細胞を96ウェルプレートに1ウェルあたり20,000細胞で播種し、回収48時間前に0.5 µg/mLドキシサイクリンおよび0.25 nM Shield1で刺激しました。全RNAを抽出し、ASCL1および下流のDelta遺伝子標的であるDLL1およびDLL3についてRT qPCRにより相対遺伝子発現量を測定しました。各遺伝子の相対発現量は、ACTBをハウスキーピング遺伝子としてΔΔCq法により算出し、NTCに対してノーマライゼーションしました。ASCL1の活性化は、神経発生において保存された重要な過程であり、Notchシグナル伝達の活性化および一部の神経前駆細胞における未分化状態の維持に関与しています。ドキシサイクリンおよびShield1刺激によりASCL1が強力に活性化され、その結果DLL3およびDLL1の発現が顕著に上昇しました。一方、ASCL1の低レベルなバックグラウンド活性化は、DLL1およびDLL3の発現に有意な影響を与えませんでした。
- Bhaya, et al., CRISPR-Cas systems in bacteria and archaea: versatile small RNAs for adaptive defense and regulation. Annu. Rev. Genet. 45, 273-297 (2011).
- M. Jinek, et al., A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity. Science. 337, 816-821 (2012).
- L.S. Qi, et al., Repurposing CRISPR as an RNA-guided platform for sequence-specific control of gene expression. Cell. 152, 1173-83 (2013).
- L.A.Gilbert, et al., CRISPR-mediated modular RNA-guided regulation of transcription in eukaryotes. Cell. 154, 442-51 (2013).
- A.W. Cheng, et al., Multiplexed activation of endogenous genes by CRISPR-on, an RNA-guided transcriptional activator system. Cell Res., 23, 1163-71 (2013).
- L. A. Gilbert, et al., Genome-Scale CRISPR-Mediated Control of Gene Repression and Activation. Cell. 159, 647–661 (2014).
- M. E. Tanenbaum, et al., A protein-tagging system for signal amplification in gene expression and fluorescence imaging. Cell. 159, 635–646 (2014).
- S. Konermann, et al., Genome-scale transcriptional activation by an engineered CRISPR-Cas9 complex. Nature. 517, 583–588 (2015).
- R. Loew, et al., Improved Tet-responsive promoters with minimized background expression. BMC Biotechnol. 10, 81 (2010).
- Banaszynski, Laura A et al., A rapid, reversible, and tunable method to regulate protein function in living cells using synthetic small molecules. Cell. 126, 995-1004 (2006).
- Egeler, Emily L et al., Ligand-switchable substrates for a ubiquitin-proteasome system. The Journal of Biological Chemistry. 286, 31328-36 (2011).
- M. A. Horlbeck et al., Compact and highly active next-generation libraries for CRISPR-mediated gene repression and activation. eLife. 5, e19760 (2016).
- Maynard-Smith, Lystranne A et al., A directed approach for engineering conditional protein stability using biologically silent small molecules. The Journal of Biological Chemistry. 282, 24866-72 (2007).
LentiBOOST™レンチウイルストランスダクションエンハンサーは、レンチウイルススピンフェクションの有無にかかわらず使用可能な独自処方のトランスダクション試薬です。細胞生存率を維持しながら、ウイルス導入効率を向上させることができます。患者由来の貴重な初代細胞や複雑な動物モデルの構築において特に有用であり、トランスダクション効率の向上により、各編集・導入ステップの成功率を高め、時間およびコスト削減につながります。また、LentiBOOST技術はすでに複数の臨床段階治療法の製造に使用されており、臨床応用を見据えたワークフローへの適用可能性を示しています。
LentiBOOSTはDharmacon試薬カタログから購入可能です。
LentiBOOST技術の詳細については、Revvity LentiBOOSTウェブページをご覧ください。
Supporting Data
LentiBOOST™ Lentivirus Transduction Enhancerを用いたCD8+ T細胞SMARTvector™ shRNAレンチウイルスシステムのトランスダクション効率向上
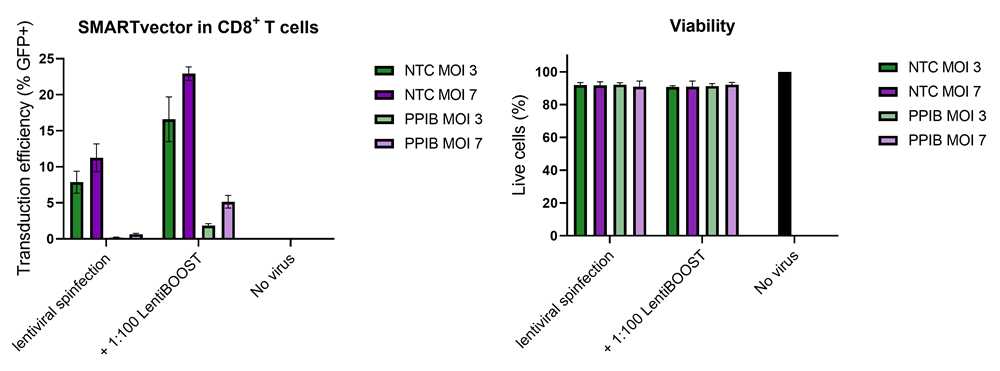
100,000個のヒト初代CD8+ T細胞に、NTCまたはPPIBを標的とするSMARTvector™ mCMV tGFPレンチウイルスコントロール粒子を、30,000 TU(MOI 3、緑)または70,000 TU(MOI 7、紫)で、1:100希釈のLentiBOOSTトランスダクションエンハンサーとともに導入しました。細胞は32 °C、800 x gで1時間遠心後、4時間培養し、その後レンチウイルス粒子およびトランスダクションエンハンサーを除去しました。トランスダクション効率(生細胞中のGFP陽性率)および細胞生存率は、トランスダクション5日後にフローサイトメトリーで評価しました。LentiBOOST技術の添加により、細胞生存率に大きな影響を与えることなく、トランスダクション効率が顕著に向上しました。
LentiBOOST™ Lentivirus Transduction Enhancerを用いたCD4+およびCD8+ T細胞Edit R™ All in one sgRNA/Cas9レンチウイルスシステムのトランスダクション効率向上
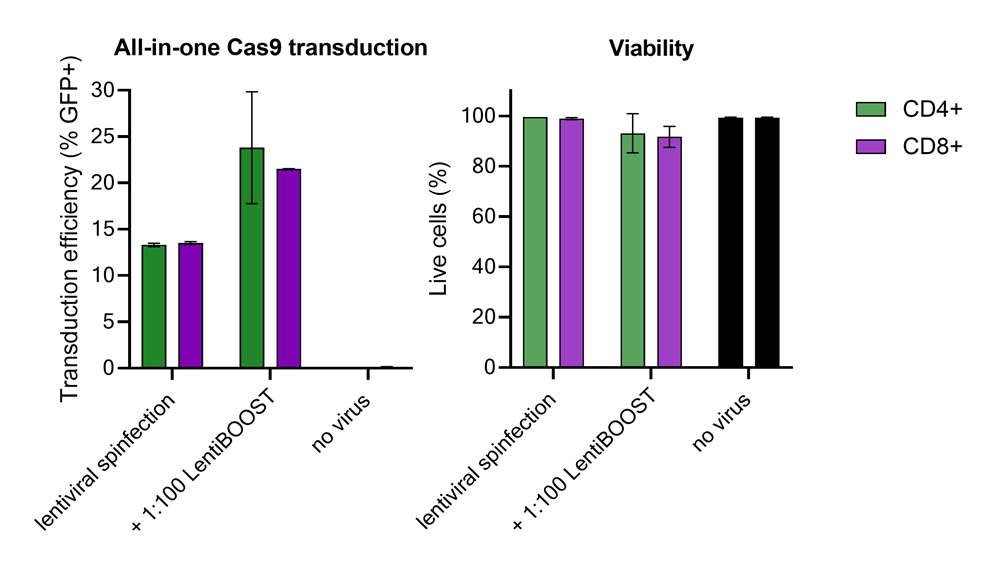
2名のドナー由来の100,000個のヒト初代CD4+およびCD8+ T細胞に、Edit R GFP DeliveryコントロールmCMVを250,000 TUで、1:100希釈のLentiBOOSTトランスダクションエンハンサーとともに導入しました。細胞は32 °C、800 x gで1時間遠心後、一晩培養し、その後レンチウイルス粒子およびトランスダクションエンハンサーを除去しました。トランスダクション効率および細胞生存率は、トランスダクション72時間後にフローサイトメトリーで評価しました。LentiBOOST技術の添加により、細胞生存率に大きな影響を与えることなく、トランスダクション効率が顕著に向上しました。
LentiBOOST™ Lentivirus Transduction Enhancerを用いたStrict R™ Inducible CRISPRaレンチウイルスシステムによるヒト人工多能性幹細胞(hiPSC)のトランスダクション効率向上

10,000個のWTC hiPSCに、Strict R™ Inducible EGFP dCas9 VPRレンチウイルス粒子を20,000 TU(MOI 2、緑)または40,000 TU(MOI 4、紫)で、1:100希釈のLentiBOOSTトランスダクションエンハンサーとともに導入しました。細胞は32 °C、800 x gで1時間遠心後、一晩培養し、その後レンチウイルス粒子およびトランスダクションエンハンサーを除去しました。トランスダクション効率および細胞生存率は、トランスダクション72時間後にフローサイトメトリーで評価しました。LentiBOOSTの添加により、細胞生存率に大きな影響を与えることなく、トランスダクション効率が顕著に向上しました。
Protocols
Safety data sheets
Related Products
ヒトおよびマウスモデルの非常に効率的な遺伝子転写活性化のためのデザイン済みCRISPRa lentiviral sgRNA
LentiBOOST transduction enhancer can increase successful viral transduction in challenging to transduce cells, or, complex cellular engineering work; while preserving cell viability and minimizing the amount of viral particles required for your experiment. LentiBOOST technology is actively used in the production of clinical stage lentivirally delivered therapies, including some approved therapies, providing a direct path to therapeutic applicability for your research studies. Tested with Dharmacon Lentiviral reagents.
レンチウイルスsgRNAコンストラクトはバイオインフォマティクスに基づいて設計され、ヒトやマウスのゲノムのどの遺伝子も標的としないことが検証されています。
遺伝子転写活性化実験の最適化と遺伝子活性化効率の確認のための検証済みのlentiviral sgRNAポジティブコントロール

