Strict R Inducible Cas9レンチウイルスシステム
精密な遺伝子ノックアウトを可能にする二重誘導制御:仕組み
System OFF:誘導剤非存在下での厳密な制御
ドキシサイクリンおよびShield1が存在しない場合、本システムは不活性状態を維持します。TRE3Gプロモーターからの最小限の転写リークによりデグロンタグ付きCas9が産生される場合でも、当該Cas9は速やかにプロテアソームによって分解されるため、バックグラウンドのゲノム編集活性は最小限に抑えられます。
System ON:制御された高効率ゲノム編集
ドキシサイクリンを添加すると、TRE3Gプロモーターからの強力な転写が誘導されます。さらにShield1を同時に添加することで、デグロンタグ付きCas9タンパク質が安定化され、標的特異的sgRNAの存在下で高効率かつ精密な遺伝子ノックアウトが可能になります。
この二重レベルの制御により、遺伝子編集実験において厳密な時間制御が実現されます。
Highlights
- 低分子誘導によるCas9発現を用いた、遺伝子編集の厳密かつ調整可能な制御
- Cas9ヌクレアーゼによる、高効率かつ高忠実度なDNA切断と、最小限のオフターゲット効果
- ドキシサイクリンおよびShield1の添加によりCas9の誘導発現および安定化を可能にするTet デグロンシステムの統合
- 単一のレンチウイルスベクターによるデリバリーで、既存の実験ワークフローへの容易な組み込みが可能
- 機能喪失研究、機能ゲノミクス、スクリーニング用途に適した、高品質かつ精製済みレンチウイルス粒子(≥1×10⁷TU/mL)を提供し、細胞毒性を最小限に抑制
- 実験設計に応じて選択可能な、ハイグロマイシン耐性、ブラスティシジン耐性、またはEGFP蛍光レポーターオプション
Strict R Inducible Cas9レンチウイルスベクターの模式図
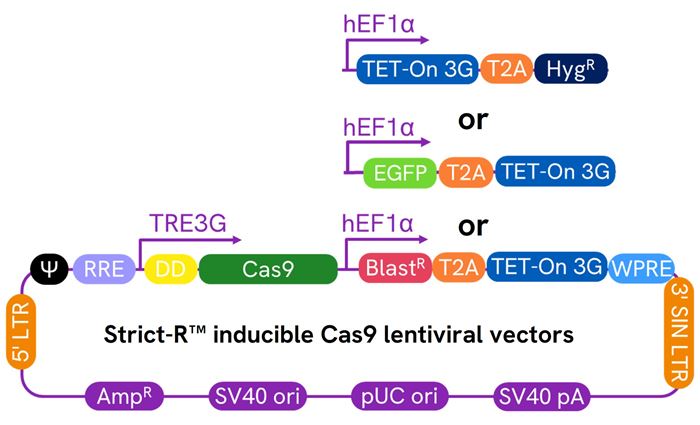
Strict R™ Inducible Cas9レンチウイルスシステムによる転写および翻訳後制御

Dharmacon™ Strict R™ Inducible Cas9 レンチウイルスシステムの模式図を示しています。ドキシサイクリンおよびShield1非存在下では、本システムは「OFF」状態となります。TRE3Gプロモーターからのリーキーな転写により、FKBP12由来の不安定化ドメイン(デグロン)と融合したCas9が翻訳されますが、当該タンパク質は速やかにプロテアソーム分解を受けます。ドキシサイクリンの添加によりTRE3Gプロモーターからの強力な転写が誘導され、さらにShield1の添加によってCas9タンパク質が安定化されます。これにより、遺伝子特異的sgRNAの存在下で、強力な標的遺伝子編集およびノックアウトが可能になります。本図はBioRender.comを用いて作成されています。
Strict R™ Inducible Cas9レンチウイルスシステムを用いた遺伝子編集ワークフロー

Strict R™ Inducible Cas9レンチウイルスシステムを用いた遺伝子編集ワークフロー
Dharmacon™ Strict R™ Inducible Cas9レンチウイルスシステムにおける低リーク性の検証
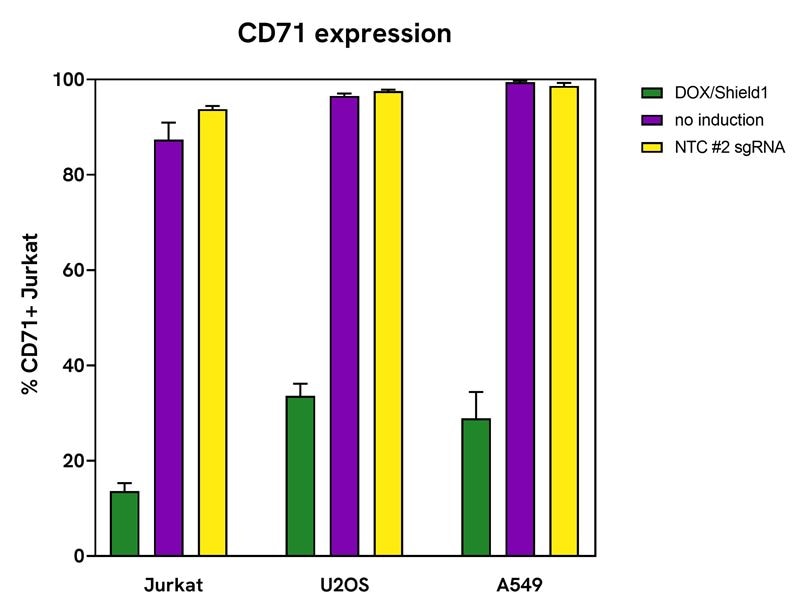
Jurkat、U2OS、A549細胞にDharmacon™ Strict R™ Inducible Hygromycin Cas9 レンチウイルスシステムを導入し、CD71を標的とするEdit RレンチウイルスsgRNA(VSGH12605 257052386)または非標的コントロールsgRNA #2(VSGC12626)をMOI 0.3でトランスダクションしました。24時間後、2 µg/mLピューロマイシンで5日間選択を行いました。Jurkat細胞は96ウェルプレートに1ウェルあたり50,000細胞、U2OSおよびA549細胞は20,000細胞で播種しました。すべての細胞に500 ng/mLドキシサイクリンおよび500 nM Shield1を添加する条件、または無処理条件で6日間培養しました。6日目に細胞を回収し、フローサイトメトリーにより受容体ノックアウト解析を実施しました。sgRNAを導入したJurkat、U2OS、A549細胞はFITC標識抗ヒトCD71抗体(1:25)で染色しました。非標的コントロールsgRNAを導入した細胞は、CD71発現が維持された対照群として用い、未処理(非誘導)条件に基づいて受容体の陽性および陰性ゲートを設定しました。
Dharmacon™ Strict R™ Inducible Cas9レンチウイルスシステムは、TRE3G単独制御のEdit R Inducible Cas9と同等またはそれ以上の性能を示す

Jurkat細胞に、Tet制御のみのEdit R™ Inducible Cas9(hEF1a BlastR)システム、またはDharmacon™ Strict R™ Inducible Blasticidin Cas9もしくはHygromycin Cas9レンチウイルスシステムを発現させました。これらの細胞に、CD28(VSGH12605 256966516)またはCD71(VSGH12605 257052386)を標的とするEdit RレンチウイルスsgRNA、あるいは非標的コントロールsgRNA #2(VSGC12626)をMOI 0.3でトランスダクションしました。24時間後、2 µg/mLピューロマイシンで5日間選択を行いました。細胞は96ウェルプレートに1ウェルあたり50,000細胞で播種し、500 ng/mLドキシサイクリンおよび500 nM Shield1を添加する条件、または無処理条件で6日間培養しました。6日目に細胞を回収し、フローサイトメトリーにより受容体ノックアウト解析を実施しました。sgRNAを導入したJurkat細胞は、PE標識抗ヒトCD28抗体(1:100)またはFITC標識抗ヒトCD71抗体(1:25)で染色しました。非標的コントロールsgRNAを導入したJurkat細胞は、受容体発現が維持された対照群として用い、未処理(非誘導)条件に基づいて受容体の陽性および陰性ゲートを設定しました。
A549細胞におけるStrict R Inducible Hygromycin Cas9レンチウイルスシステムのゲノム編集活性(ドキシサイクリン+Shield1誘導72時間後)

A549細胞に、ハイグロマイシン耐性を有するDharmacon™ Strict R™ Inducible Cas9レンチウイルスシステムを導入しました。14日間のハイグロマイシン選択後、PPIB陽性コントロール(VSGH12671)、CD71/TFRC(VSGH12605 257052386)、またはCD58/LAF 3(VSGH12605 256231081)を標的とするEdit Rデザイン済みレンチウイルスsgRNAをMOI 0.3でトランスダクションしました。さらに5日間、2 µg/mLピューロマイシンで選択を行い、TETシステム対応A549培地を使用しました。ゲノム編集実験では、二重選択後のA549細胞株を96ウェルプレートに1ウェルあたり20,000細胞で、各誘導条件につき重複で播種しました。誘導条件は、500 ng/mLドキシサイクリン+500nM Shield1、500 ng/mLドキシサイクリン単独、500nM Shield1単独、または無添加条件としました。誘導72時間後に細胞を回収・溶解し、ゲノムDNAを抽出しました。T7エンドヌクレアーゼI(T7EI)によるDNAミスマッチ検出アッセイおよびSangerシーケンスによるTIDE解析を実施しました。
A:A549細胞における標的遺伝子PCR産物をT7EIで消化後、FastRuler Low Range DNA Ladderを用いて電気泳動を行いました。下段の棒グラフは、T7EI計算ツールを用いてミスマッチアッセイによるゲノム編集率を定量した結果を示しています。
B:TIDE解析によるインデル発生率の定量結果を示しています。
Robust gene editing and minimal leakiness with Dharmacon™ Strict-R™ Inducible Cas9 Lentiviral System in two cancer cell lines
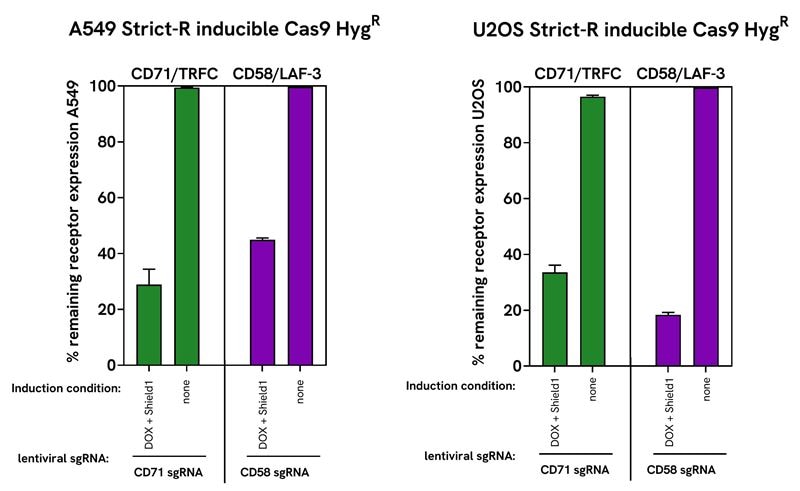
A549 were transduced with Dharmacon™ Strict-R™ inducible Cas9 lentiviral system with hygromycin resistance. After 14 days of hygromycin selection cells were transduced at an MOI of 0.3 with Edit-R pre-designed lentiviral sgRNA targeting PPIB positive control (VSGH12671), CD71/TFRC (VSGH12605-257052386) or CD58/LAF-3 (VSGH12605-256231081). Cells were selected for an additional 5 days with 2 μg/mL puromycin in TET-system approved A549 medium. For the gene editing experiment, double-selected A549 cell lines were plated in a 96-well plate at 20,000 cells/well in duplicate per induction condition: 500 ng/mL doxycycline + 500 nM Shield1, 500 ng/mL doxycycline alone, 500 nM Shield1 alone or no supplement to A549 medium (none). Cells were collected and lysed at 72 hours post induction to isolate genomic DNA for DNA mismatch detection assay with T7EI and Sanger sequencing with TIDE analysis. A. Gel electrophoresis (with FastRuler Low Range DNA Ladder) of T7EI endonuclease digested PCR products corresponding to gene target in A549. Below, in bar graph, is the quantification of T7EI gene editing by mismatch assay using the T7EI calculator. B. Quantification of gene editing by tracking of indels by decomposition (TIDE) analysis
- D. Bhaya, et al. CRISPR-Cas systems in bacteria and archaea: versatile small RNAs for adaptive defense and regulation. Annu. Rev. Genet.45, 273-297 (2011).
- M. Jinek, et al. A Programmable Dual-RNA-Guided DNA Endonuclease in Adaptive Bacterial Immunity. Science337, 816-821 (2012).
- E. Deltcheva, et al. CRISPR RNA maturation by trans-encoded small RNA and host factor Nuclease III. Nature471, 602-607 (2011).
- P. Mali, et al. RNA-guided human genome engineering via Cas9. Science339, 823-826 (2013).
- Y. Fu, et al. High-frequency off-target mutagenesis induced by CRISPR-Cas nucleases in human cells. Nat. Biotechnol.31, 822-826 (2013).
- P.D. Hsu, et al. DNA targeting specificity of RNA-guided Cas9 nucleases. Nat. Biotechnol.31, 827-832 (2013).
- T. Wang et al. Genetic screens in human cells using the CRISPR-Cas9 system. Science343, 80-84 (2014).
- D.Y. Guschin, et al. A rapid and general assay for monitoring endogenous gene modification. Methods Mol. Biol.649, 247-256 (2010).
- L.Cong, et al. Multiplex Genome Engineering Using CRISPR/Cas Systems. Science339, 819-823 (2013).
- J.C. Kappes, X. Wu and J.K. Wakefield. Production of trans-lentiviral vector with predictable safety. Methods Mol. Med.76, 449-465 (2003).
- R.H. Kutner, X.-Y. Zhang and J. Reiser. Production, concentration and titration of pseudotyped HIV-1-based lentiviral vectors. Nat. Protoc.4, 495-505 (2009)
- Anaszynski, Laura A et al., A rapid, reversible, and tunable method to regulate protein function in living cells using synthetic small molecules. Cell. 126, 995-1004 (2006).
- Egeler, Emily L et al., Ligand-switchable substrates for a ubiquitin-proteasome system. The Journal of Biological Chemistry. 286, 31328-36 (2011).
- Maynard-Smith, Lystranne A et al., A directed approach for engineering conditional protein stability using biologically silent small molecules. The Journal of Biological Chemistry. 282, 24866-72 (2007).
LentiBOOST™レンチウイルストランスダクションエンハンサーは、レンチウイルススピンフェクションの有無にかかわらず使用可能な、独自処方のトランスダクション試薬です。細胞生存率を維持しながら、ウイルス導入効率を向上させることができます。患者由来の貴重な初代細胞や、複雑な動物モデルの構築において特に有用であり、トランスダクション効率の向上により、各編集・導入ステップの成功率を高め、時間およびコストの削減につながります。また、LentiBOOST技術はすでに複数の臨床段階治療法の製造に使用されており、臨床応用を見据えたワークフローへの適用可能性を示しています。
LentiBOOSTはDharmacon試薬カタログから購入可能です。
LentiBOOSTテクノロジーの詳細については、Revvity LentiBOOSTウェブページをご覧ください。
Supporting Data
CD8⁺T細胞SMARTvector™shRNAレンチウイルスシステムにおけるLentiBOOST™を用いたトランスダクション効率の向上
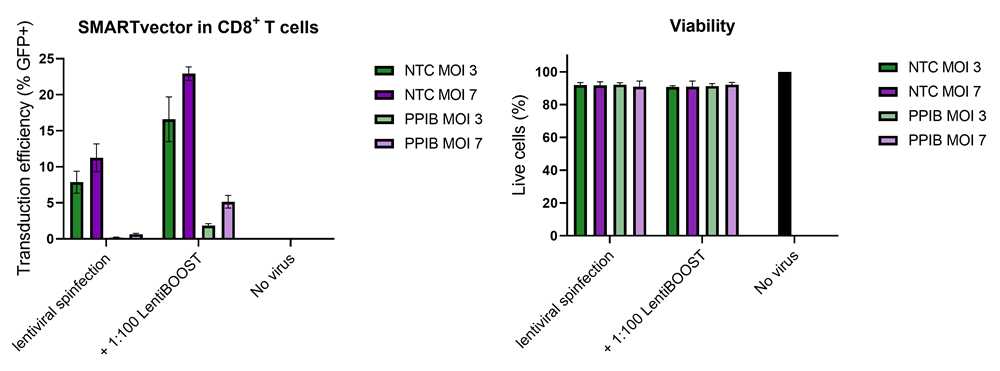
100,000個のヒト初代CD8⁺T細胞に、SMARTvector™mCMV tGFPレンチウイルスコントロール粒子(NTCまたはPPIB標的)を、30,000TU(MOI 3、緑)または70,000TU(MOI 7、紫)で、1:100希釈のLentiBOOSTトランスダクションエンハンサーとともに導入しました。細胞は32℃、800×gで1時間遠心後、4時間培養し、その後レンチウイルス粒子およびトランスダクションエンハンサーを除去しました。トランスダクション効率(生細胞中のGFP陽性率)および生存率は、トランスダクション5日後にフローサイトメトリーで評価しました。LentiBOOSTの添加により、細胞生存率に大きな影響を与えることなく、トランスダクション効率が顕著に向上しました。
LentiBOOST™レンチウイルストランスダクションエンハンサーを用いたCD4⁺およびCD8⁺T細胞におけるEdit R™ All in one sgRNA/Cas9レンチウイルスシステムのトランスダクション効率向上
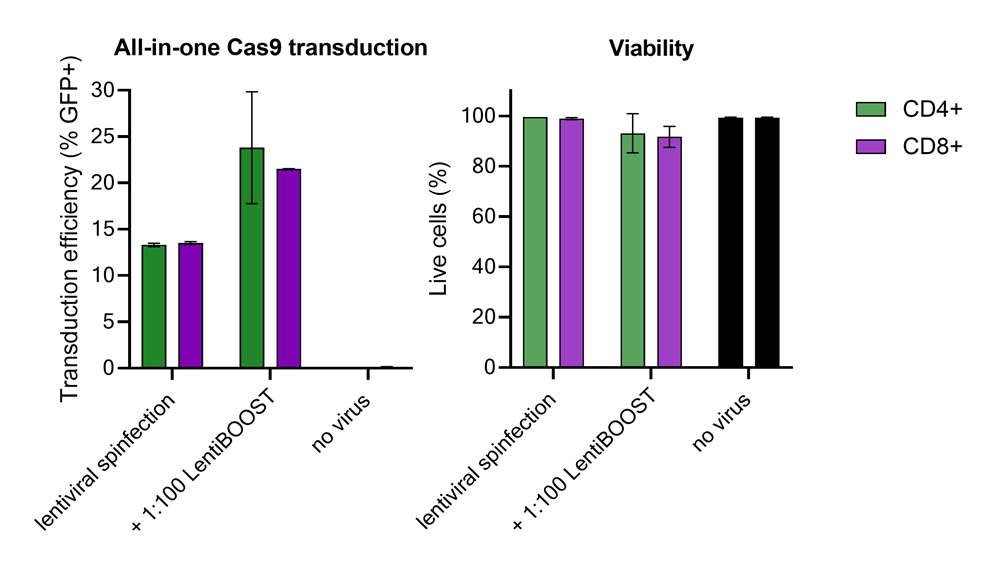
2名のドナー由来の100,000個のヒト初代CD4⁺およびCD8⁺T細胞に、Edit R GFPデリバリーコントロールmCMVを250,000 TUで、1:100希釈のLentiBOOSTトランスダクションエンハンサーとともに導入しました。細胞は32℃、800×gで1時間遠心後、一晩培養し、その後レンチウイルス粒子およびトランスダクションエンハンサーを除去しました。トランスダクション効率および細胞生存率は、トランスダクション72時間後にフローサイトメトリーで評価しました。LentiBOOSTの添加により、細胞生存率に大きな影響を与えることなく、トランスダクション効率が顕著に向上しました。
LentiBOOST™レンチウイルストランスダクションエンハンサーを用いたStrict R™ Inducible CRISPRaレンチウイルスシステムによるヒトiPSCのトランスダクション効率向上

10,000個のWTC hiPSCに、Strict R™ Inducible EGFP dCas9 VPRレンチウイルス粒子を20,000TU(MOI 2、緑)または40,000TU(MOI 4、紫)で、1:100希釈のLentiBOOSTトランスダクションエンハンサーとともに導入しました。細胞は32℃、800×gで1時間遠心後、一晩培養し、その後レンチウイルス粒子およびトランスダクションエンハンサーを除去しました。トランスダクション効率および細胞生存率は、トランスダクション72時間後にフローサイトメトリーで評価しました。LentiBOOSTの添加により、細胞生存率に大きな影響を与えることなく、トランスダクション効率が顕著に向上しました。
Protocols
Safety data sheets
Related Products
LentiBOOST transduction enhancer can increase successful viral transduction in challenging to transduce cells, or, complex cellular engineering work; while preserving cell viability and minimizing the amount of viral particles required for your experiment. LentiBOOST technology is actively used in the production of clinical stage lentivirally delivered therapies, including some approved therapies, providing a direct path to therapeutic applicability for your research studies. Tested with Dharmacon Lentiviral reagents.
